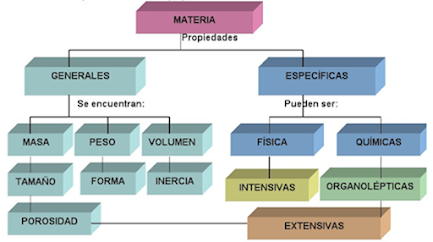
TEMA 2: Identificación de las propiedades físicas de los materiales:
• Cualitativas • Extensivas •
Intensivas
Aprendizaje esperado:
• Clasifica diferentes materiales con base en su estado de agregación e
identifica su relación con las condiciones físicas del medio. • Identifica las
propiedades extensivas (masa y volumen) e intensivas (temperatura de fusión y
de ebullición, viscosidad, densidad, solubilidad) de algunos materiales. •
Explica la importancia de los instrumentos de medición y observación como
herramientas que amplían la capacidad de percepción de nuestros sentidos.
Una propiedad física es cualquier propiedad
que es medible, usualmente se asume que el conjunto de propiedades
físicas define el estado de
un sistema físico. Los cambios en las propiedades
físicas de un sistema describen sus transformaciones y su evolución temporal
entre estados instantáneos. Las propiedades físicas a veces se denominan observables.
Podemos definir las propiedades físicas de un objeto mediante la observación y
la medición. Por ejemplo, las propiedades físicas de un cubo de madera serían: denso,
sólido, cuadrado, de madera, orgánico, no maleable, etc.
Las propiedades físicas constantemente se clasifican
en propiedades intensivas y extensivas.
Una propiedad intensiva no depende del tamaño de la extensión del
sistema, o de la cantidad de material del sistema, mientras que una
propiedad extensiva exhibe un
comportamiento agregativo o aditivo. Estas clasificaciones sólo pueden
mantenerse válidas cuando las subdivisiones más pequeñas de la muestra no
interaccionan entre sí en un determinado proceso físico o químico. Las propiedades también pueden ser
clasificadas respecto a su distribución geométrica en homogéneas y heterogéneas.
Propiedades físicas
de la materia
Las propiedades físicas de la materia son las características visibles
y propias de una sustancia que pueden ser medidas y no producen nuevas
sustancias químicas. Algunas de las propiedades físicas que podemos encontrar
son, por ejemplo:
- Estado físico: sólido líquido,
gaseoso o plasma (estados de la
materia)
- Olor: fragante, frutal, químico,
mentolado, dulce, leñoso, podrido, cítrico, etc.
- Sabor: salado, ácido, amargo,
dulce, picante.
- Densidad: relación entre masa y
volumen.
- Viscosidad: resistencia en la
fluidez de un líquido.
- Maleabilidad: flexibilidad.
- Temperatura de ebullición:
temperatura necesaria para que lo líquido se vuelva gaseoso.
- Punto de fusión: temperatura
necesaria para que los sólidos se fundan y los líquidos se solidifiquen.
- Conductividad: capacidad de
conducir algún tipo de energía.
- Solubilidad: capacidad de una sustancia de disolverse en otra, etc.
¿Qué son
las propiedades generales de la materia?
Cuando hablamos de
las propiedades generales de la materia nos
referimos al conjunto de características o cualidades físicas que
posee la materia, que está compuesta por alguna (o más de una) sustancia. Esto significa que
todo lo que existe y que podemos tocar o percibir está hecho de materia en
alguno de sus cuatro estados de agregación: sólidos, líquidos, gases y plasmas.
A pesar de estar
compuesta a menudo por distintos elementos químicos en
distintas proporciones, la materia existe de manera homogénea (no se
distinguen a simple vista sus elementos) o heterogénea (se
perciben fácilmente sus elementos). Y dependiendo de su composición,
variarán también sus propiedades físicas y químicas.
Propiedades
extrínsecas o generales. Son aquellas características que comparte
absolutamente toda la materia, sin distinción de su composición, forma,
presentación o elementos constitutivos. Las propiedades generales no
permiten diferenciar una sustancia de otra. Algunas propiedades extrínsecas son
la masa, el volumen, el peso y la temperatura.
Masa: La
masa de los objetos es la cantidad de materia que hay congregada en ellos, es
decir, la cantidad de materia que los compone. La masa se determina
mediante la inercia que
presenten o la aceleración que
presente una fuerza actuando sobre ellos, y se mide en el Sistema
Internacional con unidades de masa, como los gramos (g) o kilogramos
(kg). No debe confundirse la masa con el peso (que es una
magnitud vectorial, medida en Newtons), ni con la cantidad de sustancia (que se
mide en moles).
Peso: El peso es la medida de la fuerza que
ejerce la gravedad sobre
los objetos. Se mide en Newtons (N) en el Sistema Internacional, porque se
trata de una fuerza que ejerce el planeta sobre la materia, y
es una magnitud vectorial, dotada de sentido y dirección. El peso de un cuerpo
depende solo de su masa y de la intensidad del campo gravitacional al
cual esté sometido.
Elasticidad: Esta
propiedad permite a los cuerpos recuperar su forma original (memoria de forma)
luego de haber sido sometidos a una fuerza externa que los obligara a perderla
(deformación elástica). Es una propiedad que permite distinguir entre
los elementos elásticos y los frágiles, es decir, entre los que recuperan
su forma una vez eliminada la fuerza externa y aquellos que se fracturan en
pedazos más pequeños.
Inercia: La
inercia es la resistencia de la materia a modificar la dinámica de
sus partículas frente
a una fuerza externa. Es la propiedad de los cuerpos de permanecer en reposo
relativo o mantener su movimiento relativo
cuando no hay una fuerza externa que actúe sobre ellos. Existen dos
tipos de inercia: la mecánica, que depende de la cantidad de masa, y la
térmica, que depende de la capacidad calorífica y la conductividad térmica.
Volumen: El
volumen es una magnitud escalar que refleja la cantidad de espacio
tridimensional que ocupa un cuerpo. Se mide en el Sistema Internacional
mediante metros cúbicos (m3) y se calcula multiplicando la longitud de un
objeto, el ancho y su altura.
Dureza: La
dureza es la resistencia que ejerce la materia frente a
alteraciones físicas como el rayado, la abrasión o la penetración. Depende
de la fuerza de unión de sus partículas. Así, los materiales duros tienden a
ser impenetrables e inmodificables, mientras que los blandos pueden deformarse
con facilidad.
Densidad: La densidad alude a la
cantidad de materia presente en un material, pero también a qué tan juntas
se encuentran sus partículas. Por eso, se la define como la masa dividido el
volumen que ocupa esa masa. Los materiales densos son impenetrables y poco
porosos, mientras que los poco densos pueden ser atravesados con facilidad
porque hay espacios abiertos entre sus moléculas. La unidad estándar
de medición de la densidad es de peso por volumen, es decir, kilogramos sobre
metro cúbico (kg/m3).
PROPIEDADES ESPECIFICAS DE LA MATERIA
Las propiedades
específicas de la materia, son aquellas propiedades que caracterizan a una
sustancia y que la hace diferente de las demás. Por la forma en que se
comportan los cuerpos frente a fuerzas que se le aplican, se clasifican en
cuatro grupos llamados estados de agregación o estados físicos. Todas las
sustancias se pueden presentar en los cuatro estados de agregación dependiendo
de las condiciones de presión y temperatura a que se encuentren.
ESTADO SOLIDÓ: Presentan el estado
solidó aquellos cuerpos que tienen forma y volumen definido o propio, resisten
a los agentes que tienden a cambiar su forma y volumen, debido a que entre sus
moléculas existe una gran fuerza de atracción.
ESTADO LÍQUIDO: Presentan el
estado líquido aquellos cuerpos que tienen volumen propio o definido, que
adoptan la forma del recipiente que los contiene, resisten a los agentes que
tienden a cambiar su volumen, pero no así a los agentes que tienden a cambiar
su forma, esto debido a que la fuerza de atracción y fuerza de repulsión entre
moléculas son muy parecidas.
ESTADO GASEOSO: Presentan el
estado gaseoso, aquellos cuerpos que toman la forma y volumen del recipiente
que los contiene, por lo mismo no resisten a los agentes que cambian su forma y
volumen, esto se debe a que la fuerza de atracción entre sus moléculas es muy
pequeña en comparación a su fuerza de repulsión.
ESTADO PLASMA: Es la menos
común para la experiencia cotidiana, puede considerarse como el estado normal
de la materia en el universo, el sol, las estrellas y materia intergaláctica,
si el vapor se calienta a temperaturas superiores a 2000 oC los átomos se
disocian formando un gas de electrones libres y núcleos puros llamados PLASMA.
DENSIDAD ABSOLUTA o MASA
ESPECIFICA: La densidad de un material se define como la cantidad de masa
por unidad de volumen, por lo que se cuantifica por el cociente que resulta
entre la masa y el volumen del cuerpo.
¿Qué es medir?
La palabra medir hace referencia al acto de comparar una cantidad determinada de algo con una unidad de
medida, en donde se establece cuántas veces esta unidad ocupa un lugar
dentro de dicha cantidad.
Definición de medir: Determinar la longitud, volumen, extensión, o capacidad de una
cosa por comparación con una unidad de medida establecida que es utilizada como
referencia, usualmente mediante
algún instrumento graduado con dicha unidad.
Magnitudes fundamentales:
Son aquellas que se miden directamente, con la longitud, la masa y el tiempo.
Magnitudes derivadas:
Dependen de las fundamentales: área, volumen densidad, velocidad, etc.
Patrón: Es una base fija de comparación establecida de manera
arbitraria y representa el tamaño de una unidad de medición. El patrón para
medir longitudes o distancias es el metro; para la masa, el kilogramo; para el
tiempo el segundo
¿Qué son las medidas de peso?
Las medidas de peso son las unidades empleadas convencionalmente para calcular el peso de un cuerpo, es decir, la cantidad de materia que hay en él. Aunque más
comúnmente se conozca a esta magnitud como «peso», en realidad hablamos
de masa; ya que el primero será la medida en que, bajo la acción de
la gravedad, el objeto imprima
una fuerza sobre la
superficie en que repose y, por lo tanto, se mide en Newtons (N).
La masa, en
cambio, responde a la cantidad de materia de un objeto y para medirla se
emplean las medidas convencionales de gramo (g) y kilogramo (kg), entre
otras. La medida de peso a usar, en todo caso, dependerá de muchas
variables científicas y culturales, de modo que en algunas naciones se emplea un sistema y en otras se emplea otro. Para
llevar a cabo mediciones de
este tipo, en todo caso, se emplea una balanza: en un extremo o platillo se
coloca el objeto y del otro lado cargas equivalentes a su peso.
De acuerdo al Sistema Internacional, la medida estándar de peso es el gramo (g), tomado del
sistema métrico decimal junto a su extensa lista de múltiplos: decagramo (Dg),
hectogramo (Hg) y kilogramo (Kg) que representan 10, 100 y 1000 gramos netos
respectivamente. Por debajo, en cambio, hay también submúltiplos conocidos:
decigramo (dg), centigramo (cg) y miligramo (mg). Un gramo se definió alguna vez como la masa
de un centímetro cúbico de agua a
3,98 °C de temperatura.
Unidad de medida. Por otro lado, dentro de lo que concierne al término medir, encontramos el concepto de unidad de medida. La unidad de medida es el patrón a seguir para realizar la medición. Debe cumplir ciertas condiciones, las cuales son:
- Una unidad debe de
ser universal
- Una unidad debe ser
de fácil reproducción
- Una unidad debe ser
inalterable
- El área y el volumen de solidos regulares
se pueden calcular tomando dimensiones lineales y aplicándolas a fórmulas
matemáticas que existen para tal efecto.
- En el caso de polígonos irregulares se
utiliza el método que consiste en descomponer el polígono en triángulos,
calculando el área de cada uno y sumarlos.
- El volumen de solidos irregulares se
pueden obtener por desplazamiento de un recipiente de volumen conocido. El
volumen de agua desplazada corresponde al volumen del objeto que se quiere
saber.
- El peso de solidos se obtiene utilizando
dispositivos como la balanza y el dinamómetro.
Medición de líquidos:Los volúmenes de líquidos pueden determinarse utilizando una gran variedad de utensilios y recipientes que se fabrican actualmente para tal efecto, por ejemplo, los botes de litro empleados en las lecherías, probetas graduadas, pipetas, matraces, vasos de precipitados, etc.
Medición de gases:Los gases deben ser medidos en recipientes cerrados. Su peso varía de acuerdo con la presión que se ejerza sobre el gas y el volumen no puede ser constante por su capacidad de expansión.
Instrumentos de medición
Para medir longitud:
Cinta métrica. Regla graduada. Calibre. vernier. micrómetro. reloj comparador.
interferómetro. odómetro.
Actividad
Escribe
en tu cuaderno el siguiente cuestionario, el cual lo responderás de la
información que te proporcione.
1.-
¿Qué es una propiedad especifica de la materia?
2.-
¿Cuáles son los estados de agregación en que se encuentra la materia?
3.-
¿Describe densidad Absoluta?
4.-
¿Menciona las propiedades generales de la materia?
5.-
¿Menciona las propiedades particulares de la materia?
6.-
Dibuja o imprime el instrumento que utilizarías en un laboratorio para pesar la
masa de los cuerpos, el cual se emplea también para pesar las tortillas.
7.-
¿Qué es medir?
8.-
¿Qué son las medidas de peso?
9.- Dibuja los instrumentos que
comúnmente se emplean para medir el volumen de los líquidos.
Actividad: Midiendo
el volumen de un solido
Para la siguiente actividad necesitaras los siguientes
materiales, una regla, plastilina, una hoja de maquina o de tu cuaderno, y
elabora con ayuda de tu regla figuras geométricas las cuales pueden ser
triángulos, rectángulos, cuadrados, esferas.
1.- Investiga la fórmula para que obtengas el volumen de las
figuras que realizaras con la plastilina y la hoja de papel.
Formula del cubo:
Formula del triángulo:
Formula del Rectángulo:
Formula de la esfera:
2.- Con la plastilina elabora 5 esferas, cada una de
diferente tamaño y con su fórmula calcula su volumen y regístralo en la tabla.
3.- Con la hoja de papel realiza: 2 triángulos (uno de 3 x 5
cm y otro de 4 x 6 cm) 2 cubos (3 x 3 cm y 1.5 x 1.5 cm) 2 rectángulos (10 x
3cm y 15 x 5 cm) y con su fórmula calcula su volumen y regístralo en la tabla,
no olvides hacer sus dibujos de cómo te quedaron las figuras geométricas
TABLA
|
FIGURA |
FORMULA |
VOLUMEN |
|
Esfera 1 |
|
|
|
Esfera 2 |
|
|
|
Esfera 3 |
|
|
|
Esfera 4 |
|
|
|
Esfera 5 |
|
|
|
Triangulo 3 x 5 cm |
|
|
|
Triangulo 4 x 6 cm |
|
|
|
Cubo 3 x 3 cm |
|
|
|
Cubo 1.5 x 1.5 cm |
|
|
|
Rectángulo 10 x 3 cm |
|
|
|
Rectángulo 15 x 5 cm |
|
|
Dibujos de las imágenes y operaciones de las mismas.
Actividad contesta el siguiente crucigrama.